Nenhum produto no carrinho.
Ultimas Noticias
TESTE DE ENDOTOXINAS – LAL – ENSAIO DE AMEBÓCITOS DE LIMULUS
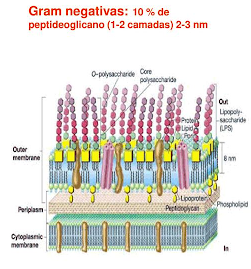
O kit de endotoxinas LAL é usado para detectar endotoxinas bacterianas (LPS=lipopolisacarídeos) de parede de bactérias Gram-negativas.
O que são as endotoxinas bacterianas?
- São componentes da membrana de bactérias Gram-Negativas; p.e. E. coli, Salmonella, etc., microrganismos amplamente distribuídos no ambiente e no intestino dos animais de sangue quente.
- As endotoxinas são agentes inflamatórios muito potentes que conservam sua atividade após a esterilização, por tanto se deve controlar a sua presença.
L.A.L.
O Teste de LAL é descrito na United States Pharmacopeia (USP) no capítulo Bacterial Endotoxin Test (Teste de Endotoxinas Bacterianas) e os capítulos equivalentes na Farmacopeia Europeia (Capítulo 2.6.14), Farmacopeia Japonesa (testes gerais, No. 4.01), Farmacopeia Brasileira, etc. Todos as Farmacopeias foram harmonizadas, portanto, o texto do procedimento é equivalente em todo o mundo.
O Reagente para Teste de LAL (Limulus Amebocyte Lysate) é um extrato aquoso das células sanguíneas (amebócitos) do caranguejo-ferradura, Limulus polyphemus. Portanto, este teste também é chamado Limulus Test.
O Teste de LAL é usado para detectar a presença de endotoxinas em produtos farmacêuticos injetáveis, produtos biológicos, dispositivos médicos (correlatos), etc. Ele também é usado nas unidades de diálise, pesquisa e outras aplicações.
As endotoxinas bacterianas são muito resistentes e só podem ser destruídas pelo calor seco ? 250°C x 30 min. ou 180°C x 3 h.
Endotoxinas são moléculas grandes e complexas que contêm lipídeos e hidratos de carbono. A porção lipídica provoca a resposta imunológica ao entrar no sangue ou no líquido cerebrospinal; produz febre, debilidade, choque, vasodilatação, inflamação, queda da pressão e dependendo do estado imune provoca a sepse generalizada e causa a morte.
Existe um marco regulatório internacional que estabelece a obrigatoriedade da realização do Teste de LAL ou Teste de Endotoxinas Bacterianas a todos os produtos parenterais, injetáveis, correlatos (seringas, cânulas, etc.), produtos de biotecnologia, matérias primas, soluções para diálise, etc. e todos os produtos para uso humano que se encontram em contato com a corrente sanguínea ou líquido cerebrospinal os quais devem ser estéreis e apirogênicos .
Métodos do Teste de LAL
Existem três métodos principais para a realização do teste de LAL:
- Gel Clotou Método de Coagulação
- Método Turbidimétrico
- Método Cromogênico
Os Métodos Turbidimétrico e Cromogênico são quantitativos. Por se tratar de métodos fotométricos requerem um equipamento leitor óptico.
Gel Clot LAL
Teste com amostras; aplicar 100 μL da amostra
diretamente na ampola. Incubar por 1 h a 37°C.
Reação positiva: gel firme quando invertido a 180°
Reação negativa: não há formação de gel firme.
Teste semi-quantitativo, diluições seriadas ½, ¼,
1/8, 1/16 … Etc.
100 μL de cada diluição diretamente nas ampolas.

Ensaio de LAL semi-quantitativo: Ensaio Semi-Quantitativo de Gel Clot Quantificar a concentração de Endotoxinas é encontrar o ponto final em uma série de diluições de amostras. No seguinte exemplo, a amostra é diluída com água LAL Reagente, a sensibilidade da LAL é 0,125 UE/mL.
Concentração da Endotoxina
= Sensibilidade de LAL x endpoint da diluição (inverso)
= 0,125 EU/mL x 8
= 1UE/m

Assine nossa Newsletter Fique por dentro das nossas novidades e promoções exclusivas! Cadastre-se agora e não perca nenhuma atualização.